- 1
- 아타신
- 조회 수 6401
지난 칼럼에 이어 오늘은 인체용의약품의 관리시스템과 동물용으로 사용되는 인체용의약품의 관리시스템을 비교해 보고자
합니다.
1. 모든 인체용의약품은 약사법, 약사법시행규칙, 의약품 등의 안전성/유효성 심사에 관한 규정 등의 품목허가와 관련된
규정에 따라 제품에 대한 효능/효과, 용법/용량, 안전성, 제품품질(기준 및 시험방법, 안정성시험자료 등)에 대한 입증자료를 제출하여 해당 품목에 대한 허가를 취득하도록 하고 있고, 인체사용에
있어 적절한 안전성과 유효성을 확보하지 못했다고 판단되는 경우 품목허가를 받을 수 없습니다.
2. 인체용의약품 중 신약(국내에 처음 도입되는 성분을 함유한 의약품, 신성분 의약품)의 경우에는 ‘신약 등의 재심사 기준’에 따라 시판 후에도 허가된 질환별 / 환자별 유효성입증자료, 부작용발생에 대한 자료 등을 일정기간 모아 제출하도록 하고 이를 검토하여 허가사항이 변경되도록 하는 등 허가 이후에도 허가사항과 효능/용법/부작용에 있어 문제가 없는 지 재점검토록 하고 있습니다.
3. 또한 모든 국내 허가된 의약품(신약, 자료제출의약품, 허가품목, 신고품목)에 대해 ‘의약품 재평가 실시에 관한 규정’에 따라 매년 약효분류군별로 재평가대상을 지정하여 기존 허가된 허가사항 중 특히 안전성/유효성(용법/용량, 효능/효과, 부작용 등이 해당)에 대한 자료를 제출 받아 현재의 기준으로, 이미 허가된 효과를 충족할 수 없거나 문제가 있는 경우 급여제한, 재분류, 품목허가취소 등의 조치를 통해 의약품을 재평가하고 있습니다. 또한 수시로 외국의 안전성정보나 국내 부작용정보를 반영하여 절차를 거쳐 허가사항을 변경하거나 조정하고 있습니다.
4.
여러분들도 아시다시피, 병원에서 치료를 위해
약을 처방할 시에는 사용된 약과 용법에 대한 정보가 처방전을 통해 환자의 손을 거쳐 약국에 전달되어
1차 점검을 받도록 하고, 보험청구 시 국가기관인 심사평가원으로 그 처방정보가 제출되어
처방된 약에 대한 적정성을 심사를 받도록 하고 있으며, 이를 통해 과잉처방, 중복처방, 현행 급여가이드라인을 벗어난 처방 등 문제처방이나 허위청구
등의 문제가 발생할 시 과태료나 보험청구삭감을 통해 문제발생을 최소화하기 위한 시스템을 갖추고 있습니다.
5.
인체용의약품 중 처방의약품(마약, 향정신성의약품, 전문의약품, 일부
보험약가를 가진 일반의약품)을 의사가 처방하면 처방전을 발행하여 환자에게 제공되며, 환자를 이 처방전을 가지고 약사에게 조제를 의뢰하여 병원 à 환자
à 약사를 거치면서 자연스럽게 누락된 약이 없는지, 약의 변경 여부, 처방된 약이 적절히 사용되었는지 점검하도록 하고 있습니다. 또 환자본인이
원할 경우 ‘환자보관용’ 처방전을 언제든 발급받아 치료에
사용된 약의 종류와 용법 등의 정보를 손쉽게 얻을 수 있도록 하고 있습니다.
6. 또한 병원, 의원, 약국에서는 약물투여 시 부작용이 발생한 경우 27개 지역의약품안전센터(2014년 기준)를 통해 한국의약품안전관리원으로 그 부작용을 보고하도록 하고 있습니다. 참고로 약국에서 대한약사회 지역의약품안전센터를 통해 보고된 부작용 건수는 2013년 5,141건, 2014년 상반기(1월~6월) 5,372건으로 매년 증가하고 있습니다.
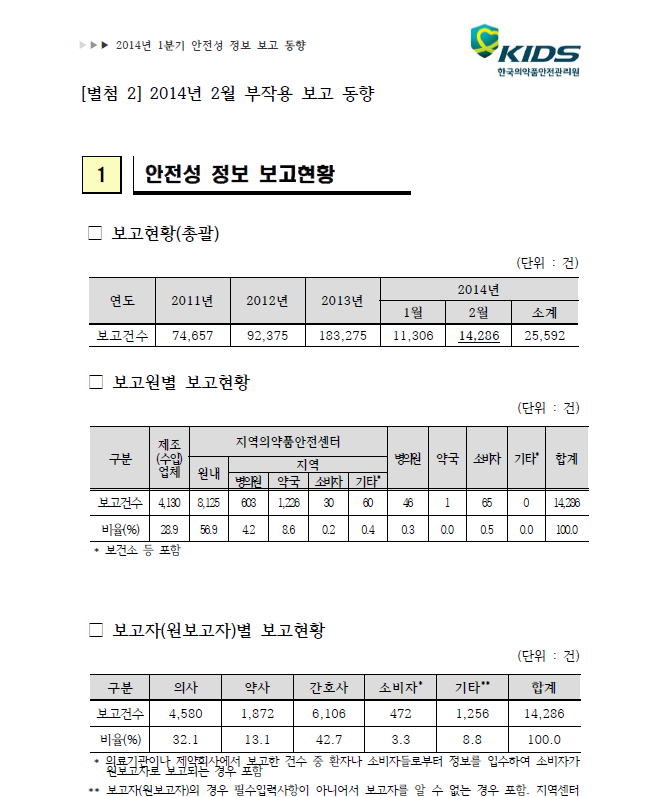
7. 요약하자면, 모든 인체용의약품은 효능/용법/안전성/안정성 등의 자료를 제출하여 허가를 받아야 하며, 허가된 이후에도 재심사나 재평가 과정을 통해 허가사항이 정기적으로 재점검되고 있으며, 실제 환자에 사용될 시에도 처방전 발행을 통한 처방정보공개, 약사의 처방검토, 심사평가원을 통한 처방 적정성 검토, 부작용보고를 통한 시판 후 안전성관리 등의 총체적 관리시스템을 갖추고 있습니다. 이러한 관리 시스템을 '약물감시 (pharmacovigilance)'라고 합니다.
이러한 모든 시스템은 사람에게 투약될 인체용의약품에 대한 오남용을 억제하도록 유도하고, 기 허가된 제품이 허가 당시 제출된 자료로 이미 효능/용법 등이
입증되었다 하더라도 시판 후에 추가로 발견된 부작용이나 기존 효능입증이 미흡할 경우 허가사항을 축소하거나 심한 경우 퇴출시켜 사람에게 투여될 의약품이
최대한 안전하게 투여되도록 엄격하게 관리하고자 함이라고 말할 수 있겠습니다.
동물용의약품에 대한 허가규정도 인체용의약품과 유사하게 약사법, 동물용의약품
등 취급규칙, 동물용의약품 등 안전성/유효성 심사에 관한
규정 등의 관련규정에 근거하여 해당제품에 대한 효능/효과, 용법/용량에 대한 근거자료를 제출하여 품목을 허가하고 있고 재평가 등의 과정을 거치도록 하고 있습니다.
하지만 동물에게 사용되는 인체용의약품의 사용에 있어서는 인체약과 비교하여 안전관리 시스템이 부족한 것으로 보입니다.
1. 일단, 인체용의약품을 마약, 향정신성의약품, 전문의약품 등을 망라하여 자유롭게 약국으로부터 구입하여
치료목적으로 사용할 수는 있으나, 동물병원에서 사용되는 인체용의약품에 대한 처방정보 공개가 의무화되어
있지 않아 동물보호자가 처방정보를 요구하더라고 이를 거부할 수 있어, 어떤 약이 어떤 용량으로 우리
아이에게 사용되고 있는지 알 수가 없는 경우가 많습니다.
2.
농림축산검역본부에 허가자료를 제출하여 허가를 받은 동물용의약품이 아니기에, 인체용의약품의 동물사용에 대해서는 당연히 그 효능과 용법, 안전성
등에 대한 입증자료가 제출되어 있지 않습니다. 물론 관련된 참고문헌이나 외국자료, 개인의 경험에 비추어 동물에 사용하고 있는 상황이라고 할 수 있겠으나, 해당제품들이
식품이 아닌, 오남용 시 위험성을 가진 안전관리가 필요한 의약품임을 고려하면 바람직하지 않으며, 어떠한 인체용의약품이 동물에 사용되고 있는지 실태나 조사자료도 없는 것으로 보입니다.
3.
당연히 허가 받은 품목이 아니므로 인체약에 적용되는 재심사나 재평가 등의 과정을 거칠 수도
없으며, 동물용의약품이 아니므로 부작용보고 의무도 없습니다.
4.
또한 동물치료는 모두 비보험으로 적용되므로 처방약에 대해 심평원을 통한 처방점검도 이루어
질 수 없습니다.
5.
요약하자면, 인체용의약품을 동물에게 사용시는
기본적으로 모든 약을 사용할 수 있으나, 처방전을 발행할 의무가 없으며, 처방된 약에 대한 적정성을 검토할 수 있는 점검시스템이 없고, 기본적으로
효능/용법/안정성입증자료 등이 제출되지 않은 상태로 사용되며, 얼마의 인체용의약품이 사용되고 있는지 그 현황이 관리되고 있지 않으며, 재평가나
부작용보고도 이루어 지지 않아, 근거자료를 통해 허가된 제품에 대해서도 문제점이 발견되면 퇴출되는 인체용의약품의
안전관리시스템에 비추어 전혀 실질적인 사후점검이 될 수 없는 상황이라 할 수 있습니다.
비록 동물용의약품이라 할지라도,
반려문화를 통해 한가족으로 취급 받고 있는 수준으로 그 문화가 성숙되어가고 있는 반면, 이렇게
아무런 규제나 제한 없이 인체용약의 사용이 허용되는 것은 의약품의 안전관리시스템을 고려하면 문제가 있다고 생각됩니다.

다음에는 이러한 인체용의약품의 동물사용이 지속될 시 우려되는
문제점 등에 대해 생각해 보도록 하겠습니다.
 포함 3명이 추천
포함 3명이 추천












![[반려동물과 음식상호작용 01] 짜장면집 강아지는 양파를 많이 먹을텐데, 괜찮은 이유가 뭘까? 양파와 반려동물에 관한 진실](http://anipharm.net/files/thumbnails/087/075/75x50.crop.jpg?20210101201458)
![[반려동물과 음식상호작용 01] 짜장면집 강아지는 양파를 많이 먹을텐데, 괜찮은 이유가 뭘까? 양파와 반려동물에 관한 진실](http://anipharm.net/files/thumbnails/087/075/210x140.crop.jpg?20210101201458)